Replication Stress Is an Actionable Genetic Vulnerability in Desmoplastic Small Round Cell Tumors (2025)
https://doi.org/10.1158/0008-5472.CAN-23-3603
Desmoplastic Small Round Cell Tumor (DSRCT)은 극히 드문 악성 육종으로, 주로 청소년기에서 젊은 성인 남성에게 발생한다. 대부분의 환자는 진단 시 이미 복강 내 다발성 전이가 있는 상태로 발견되며 5년 생존율이 15% 미만일 정도로 예후가 매우 나쁘다. 현재까지도 치료는 유잉육종(Ewing sarcoma) 치료 프로토콜을 그대로 따르고 있다. 즉, 고용량 화학요법(다제 병용)과 광범위 절제 수술, 그리고 경우에 따라 방사선치료를 병행하지만 완치 가능성은 여전히 낮다. 지난 20년 동안 이 질환에서 새로운 치료제가 등장한 적이 거의 없다는 점이 문제다.
대부분의 DSRCT는 염색체 t(11;22)(q13;q12) 전좌로 인해 EWSR1–WT1 융합 유전자(EWS–WT1)를 형성한다. 이 단백질은 전사인자로 작용하며, 세포 내 유전자 발현 조절 네트워크를 비정상적으로 바꾼다. 즉, EWSR1의 전사활성 영역과 WT1의 DNA 결합 영역이 합쳐진 형태로 암세포가 특정 유전자 집단을 과도하게 발현하도록 유도한다.
EWS–WT1은 이 암의 발생에 필수적이며 충분한 단일 발암 인자로 알려져 있다. 하지만 전사인자를 직접 약물로 억제하기는 거의 불가능하다. 이에 연구자들은 "직접 억제가 어렵다면, EWS–WT1이 만들어내는 세포 내 결과적 변화를 표적으로 삼자"는 전략을 세웠다. 그중에서도 특히 복제 스트레스(replication stress)와 DNA 손상 복구 체계의 의존성이 유력한 표적 후보로 주목됐다.
연구 방법
1) 고속 약물 감수성 스크리닝
-
DSRCT 세포주(JN1)를 대상으로 항암제 및 표적치료제 79종을 고농도부터 저농도까지 8단계 농도로 처리했다.
-
세포 생존율을 측정해 AUC(Area Under Curve)를 계산하고 다른 92개 암세포주와 비교하여 어떤 약물에 특이적으로 민감한지를 분석했다.
2) 핵심 약물군 검증
-
스크리닝 결과 유망한 약물군으로 PARP 억제제(PARPi)와 ATR 억제제(ATRi)가 선택됐다.
-
각각의 대표 약물로 탈라조파립(talazoparib), 올라파립(olaparib), AZD6738, M4344 등을 사용했다.
-
유잉육종(A673 세포)과 골육종(SaOS-2 세포)을 대조군으로 비교했다.
3) 3차원 모델 및 동물모델 검증
-
환자 복막에서 얻은 조직으로 PDX 오가노이드(3D)를 제작해 실제 종양 환경에 가까운 조건에서 약물 반응을 관찰했다.
-
또한 NSG 마우스에 JN1 세포를 이식한 이종이식 모델을 만들어 병용요법의 항종양 효과를 확인했다.
주요 결과
1) DSRCT 세포는 PARP·ATR 억제제에 예민했다
-
JN1 세포는 PARPi(탈라조파립, 올라파립)와 ATRi(AZD6738, M4344)에 모두 높은 감수성을 보였다.
-
세포 생존률 반감농도(SF50)는 실제 임상 약물 농도 범위 안에 있었다.
-
예를 들어, 탈라조파립의 SF50은 10 nM, 실제 임상 평균 혈중 농도는 약 7 nM이었다.
-
-
이는 단순한 세포 실험 결과가 아니라 실제 환자에게 적용 가능한 농도 수준임을 시사했다.
2) PARP1 단백질 발현이 치료 반응을 좌우했다
-
R 세포주는 PARPi에 내성이 있었는데, 원인은 PARP1 단백질 발현 저하였다.
-
PARP1을 siRNA로 억제하면 JN1 세포의 약물 감수성이 사라졌고 반대로 PARP1이 높은 세포는 약물에 취약했다.
→ 즉, PARP1 발현이 PARPi의 효과를 결정하는 핵심 인자였다.
3) PARP·ATR 병용 시 강한 시너지 효과
-
두 약물을 함께 썼을 때, 세포 생존률은 단독 투여보다 훨씬 낮아졌다.
-
Bliss 독립성 모델로 계산한 시너지 점수는 JN1 세포 15.7 (강한 시너지), R 세포: 3.9 (약한 상가효과)로 PARP1이 높을수록 병용 효과가 뚜렷했다.
-
환자유래 오가노이드(PDX-O)에서도 동일한 경향이 재현됐다. 3차원 모델에서는 약물 저항성이 다소 높았지만, 여전히 병용 시 세포 사멸이 강하게 일어났다.
-
동물실험(NSG 마우스)에서도 병용요법이 종양 크기를 뚜렷하게 줄였다.
-
단독 투여군 대비 종양 부피 약 60% 감소
-
일부 마우스에서는 종양 퇴축(tumor regression)까지 확인됐다.
-
4) 복제 스트레스와 DNA 손상의 누적
-
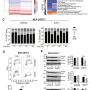
두 약물의 병용은 세포 내 γH2AX 포커스(이중가닥 손상 표지자)와 RAD51 포커스(상동재조합 복구 관련 단백질)를 모두 증가시켰다.
-
세포주기 분석 결과, G2–M 체크포인트 정지와 마이크로뉴클레이(염색체 조각 잔여물) 축적이 확인됐다.
-
이는 DNA 복제 중단 → 복제 스트레스 → 유전체 불안정성 증가 → 세포사멸의 일련의 과정을 의미했다.
5) EWS–WT1 융합 단백질이 핵심 결정자
-
EWS–WT1 발현을 siRNA로 억제하면 PARPi·ATRi 감수성이 사라졌다.
-
반대로 EWS–WT1이 존재할 때만 복제 스트레스와 DNA 손상이 일어났다.
-
이는 EWS–WT1이 R-loop 형성을 증가시켜 DNA 복제 과정을 방해하기 때문이다.
-
또한 R-loop를 해소하는 효소 RNase H1을 과발현시켰을 때도 약물 감수성이 소실됐다.
→ 즉, EWS–WT1 → R-loop 축적 → 복제 스트레스 → PARPi/ATRi 취약성의 분자 경로가 확립됐다.
6) 면역 관련 경로(cGAS–STING) 활성화
-
PARPi·ATRi 병용 시 세포 내에서 cGAS–STING 선천면역 경로가 활성화됐고 PD-L1 단백질 발현이 상승했다.
-
이는 종양이 면역세포에 더 잘 노출되도록 하는 효과로, 향후 면역관문억제제(PD-1/PD-L1 차단제)와 병용 가능성이 제시됐다.
종합 결론
-
EWS–WT1 융합 단백질이 DSRCT의 핵심 발암 요인이며, 이 단백질은 세포에 만성적인 복제 스트레스를 유발한다.
-
이러한 복제 스트레스는 세포가 ATR/CHK1 경로에 의존하게 만들며, PARP·ATR 억제제는 이 의존성을 동시에 차단해 세포 사멸을 유도한다.
-
PARP1 단백질 발현이 충분한 종양에서는 병용 효과가 극대화된다.
-
병용요법은 DNA 손상 누적뿐 아니라 면역활성화 효과도 유발해, 면역·표적 복합 치료의 가능성을 열었다.
임상적 의의
-
본 연구는 DSRCT에서 EWS–WT1 유도 복제 스트레스라는 새로운 치료 표적을 처음으로 제시했다.
-
PARP 억제제 + ATR 억제제 병용요법은 기존 항암화학요법보다 훨씬 선택적이고 분자적 근거가 명확한 전략이다.
-
특히, PARPi는 이미 여러 고형암(난소암, 유방암 등)에서 임상 승인을 받은 약물이므로, 임상 전환 속도가 빠를 가능성이 높다.
-
향후에는 PARPi·ATRi 병용을 DSRCT 1차 혹은 재발 환자 치료 임상시험으로 이어갈 필요가 있다.







 손님
손님